Det största antalet svavelsyraanläggningar använder svavel som råvara. Svavel reduceras genom en biprodukt från bearbetningen naturgas och några andra industrigaser (generator, oljeraffineringgräsmatta). Sådana gaser innehåller alltid en viss mängd svavelföreningar. Förbränning av oraffinerad naturgas från svavel leder till miljöföroreningar med svaveloxider. Därför avlägsnas vanligtvis svavelföreningar först i form av vätesulfid, som sedan delvis förbränns till SO2, varefter blandningen av vätesulfid och svaveldioxid reagerar på ett bauxitskikt vid 270-300 ° C och omvandlas som ett resultat av denna interaktion till S och H2O. Svavlet som erhålls på detta sätt kallas "gasformigt". Förutom "gas" -svavel kan nativt svavel användas som råmaterial.
Svavel som råvara för produktion av svavelsyra har ett antal fördelar. För det första innehåller den, till skillnad från pyrit, nästan inga föroreningar som kan vara katalytiska gifter vid kontaktoxidation av svaveldioxid, till exempel arsenikföreningar. För det andra, när det bränns, bildas inte fast och annat avfall som kräver lagring eller sökning efter metoder för vidare bearbetning (vid förbränning av pyrit bildas nästan samma mängd fast avfall per 1 ton initial pyrit). För det tredje är svavel mycket billigare att transportera än pyrit, eftersom det är en koncentrerad råvara.
Låt oss överväga ett "kort" schema för att erhålla svavelsyra från svavel med DKDA-metoden (fig. 2).
Figur: 2. Schema för produktion av svavelsyra från svavel med metoden dubbelkontakt och dubbel absorption:
1 - ugn för svavelförbränning; 2 - spillvärmepanna; 3 - ekonomizer 4 - startugn: 5. 6 - värmeväxlare för startugnen. 7 - kontaktanordning: 8 - värmeväxlare 9 - torktorn. 10, 11 - de första och andra monohydratabsorbatorerna. 12 - syrafångare; 13 - avgasrör.
Det smälta svavlet passerar genom nätfilter för att rengöra det från möjliga mekaniska föroreningar (svavel smälter vid en temperatur som är högre än 100 такойС, därför är denna metod för rengöring det enklaste) och skickas till ugn 1, i vilken luft tillförs som ett oxidationsmedel, tidigare torkat med svavelsyra i produktionen i torkningstornet 9. Rostgasen som lämnar ugnen kyls i spillvärmepannan 2 från 1100-1200 ° C till 440-450 C och riktas mot denna temperatur, lika med antändningstemperaturen för industriella katalysatorer baserat på vanadinpentoxid, till det första lagret i hyllkontaktapparat 7 ...
Den temperaturregim som krävs för att föra processens arbetslinje till linjen med optimala temperaturer regleras genom att leda strömmar av delvis reagerad eldgas genom värmeväxlare 8, där den kyls av uppvärmda gasströmmar efter absorption (eller torkad luft). Efter det tredje kontaktsteget kyls rostningsgasen i värmeväxlare 8 och skickas till en mellanliggande monohydratabsorberare 10, återflödas med svavelsyra som cirkulerar genom syrauppsamlaren 12 med en koncentration nära 98,3%. Efter avlägsnande av svaveltrioxid i absorbatorn 10 och den resulterande avvikelsen från den nästan uppnådda jämvikten upphettas gasen åter till antändningstemperaturen i värmeväxlarna 8 och skickas till det fjärde kontaktsteget.
I detta schema tillsätts en del av den torkade luften för att kyla gasen efter det fjärde steget och ytterligare blandning av jämvikten. De gaser som reageras i kontaktanordningen ledes för kylning genom ekonomisorn 3 och skickas till den sista 11 monohydratabsorberaren 11, från vilken gaserna som inte innehåller svaveloxider släpps ut genom avgasröret 13 till atmosfären.
För att starta installationen (bringa den till en given teknisk, i synnerhet temperatur, läge) tillhandahålls en startugn 4 och värmeväxlare för startugnen 5 och 6. Dessa anordningar stängs av efter installationen tas i drift.
Svavelsyraproduktion
Svavelsyra är den billigaste av mineralsyrorna. Dess produktion i Ryssland var 8,2 miljoner ton 1993. Egenskaper för svavelsyra: densitet - 1,85 g / cm 3 vid 0 o C;
t bal - 296 o C, blandas med vatten i alla förhållanden med frisättning av en stor mängd värme. Det är mycket kemiskt aktivt: det löser upp metalloxider och de flesta rena metaller, förskjuter alla andra syror från deras salter. Den har en hög vattenavlägsnande kapacitet. Trä och andra växt- och djurvävnader förstörs i koncentrerad svavelsyra.
Användning av svavelsyra: produktion av mineralgödselmedel, icke-järnmetallurgi, etsning av metaller, produktion av färgämnen, lacker, färger och andra organiska ämnen.
Metoder för att erhålla:
1. termisk sönderdelning av järnsulfat (upptäcktes under XIII-talet)
2. nitrisk metod (används i 200 år)
3. Kontaktmetoden (som använts i mindre än 100 år) har nu ersatt alla andra. Denna metod producerar mer än 80% svavelsyra.
Svavelsyraproduktion med kontaktmetod
De viktigaste stegen i produktionen av svavelsyra:
1.Produktion av svaveldioxid
2. Rening av svaveldioxid
3. oxidation av svaveldioxid till svavelsyraanhydrid
4 erhåller oleum
I. blir så2
Råmaterial för produktion av SO 2 - nativt svavel, pyrit, kopparpyrit; kalcium- och natriumsulfater.
Att erhålla svaveldioxid från pyrit.
Pyrit har formeln FeS 2. Upp till 40% svavelsyra erhålls från pyrit, den innehåller upp till 50% svavel och upp till 40% järn. Om pyrit innehåller en stor mängd icke-järnmetaller utsätts den för flytningsförmåga för att erhålla sulfider av icke-järnmetaller och pyrit.
För att erhålla svaveldioxid avfyras pyrit i ugnar av olika utförande. I detta fall inträffar följande reaktioner:
4 FeS 2 + 11O 2 → 2Fe 2 O 3 + 8 SO 2 + 3400 kJ
Denna process består av flera steg:
Vid temperaturer över 500 ° C dissocierar pyrit:
2 FeS 2 → 2FeS + S 2 varefter svavlet snabbt brinner ut
S2 + 2O2 → 2 SO2
Återstående FeS oxideras:
4 FeS + 7O2 → Fe203 + 4 SO2
Vid avfyrning av pyrit omvandlas 5-10% svavel till SO 3
2 SO 2 + O2 → 2SO 3
Ugnar används för att skjuta pyrit:
Mekanisk hyllaÄr mångsidiga ugnar som kan användas för avfyrning av bulkmaterial. Vid avfyrning av pyrit erhålls en gas med följande komposition: SO2-10%, O2 -9%, N2 -82%. Vid t\u003e 850 ° C sintras pyrit i bitar, vilket är oönskat. Avfyrningen utförs därför vid en temperatur av högst 850 0 C. Dammhalten i gasen är högst 10 g / m 3.
Nackdelar med mekaniska hyllugnar: de är komplexa i design och dyra, ger inte fullständig förbränning av svavel, en gas med låg koncentration av SO2 erhålls, upp till 2% svavel finns kvar i pyritkärlet.
Pulveriserade ugnarkan endast användas för torrflotationspyrit, som matas in i ugnen med ett munstycke. Förbränningen är mycket mer intensiv och möjligheten till sintring är mindre, därför kan du använda temperaturer upp till 1100 0 С - detta gör att du kan tillföra mindre överskott av luft. SO 2-koncentration ≤ 13%, upp till 1,5% svavel finns kvar i asken. Avgaserna har en temperatur på cirka 1000 ° C och matas till spillvärmepannan för att generera ånga.
Nackdelar med pulveriserade ugnar: behovet av att använda kol-chedan med låg luftfuktighet, hög dammhalt i gasen (upp till 100 g / m 3).
Fluidiserade sängugnar ochde används för att rosta både flyt och vanlig pyrit. Koncentrationen av partiklar i luftvolymen är större än i pulveriserade ugnar. Avfyrning utförs vid en temperatur av 800 ° C. Koncentrationen av SO 2 i gasen är upp till 15%, cirka 0,5% svavel finns kvar i asken. Ugnarna är enkla i design och mycket effektiva. Numera hittar de mer och mer utbredd användning.
Nackdelar med ugnar med fluidiserad bädd: hög dammhalt (upp till 200 g / m 3) behovet av att använda partiklar av liknande storlek.
Användningen av svavel för produktion av svaveldioxid.
Svavel smälts först med döv ånga, filtreras från mekaniska föroreningar och matas genom ett munstycke in i ugnen. I det här fallet avdunstar svavlet och brinner.
Förutom munstycksugnar används också cyklonugnar, där intensiteten av blandning och förbränning av svavel på grund av den tangentiella lufttillförseln är högre än i munstycksugnar. Därför ersätter för närvarande cyklonugnar munstycksugnar.
2. Rengöring av gas från damm.
Grov rengöring utförs i cykloner och dammuppsamlingskammare som installeras efter ugnarna. Efterbehandlingen utförs i tvättorn och våta elektrostatiska fällare.
3.Kontakta oxidation av svaveldioxid till svavelsyraanhydrid - t.ex.då är processen heterogen katalytisk, det vill säga reaktanterna och katalysatorn är i olika faser. I detta fall är reaktanterna gaser och katalysatorn är i fast tillstånd. Följande reaktion äger rum på katalysatorn:
2 SO 2 + O 2 ↔ 2SO 3 +190 kJ.
För att öka SO3-utbytet är det nödvändigt att öka trycket och sänka temperaturen, men när temperaturen sjunker minskar reaktionshastigheten. För att säkerställa en tillräckligt hög reaktionshastighet utförs därför processen vid en temperatur av minst 450 ° C.
Dessutom används katalysatorer. Hundratals ämnen är kända som påskyndar denna reaktion. De bästa är Pt, FeO, V205. Den mest aktiva är platina, men den är mycket dyr och lätt oxiderad av föroreningar i rostningsgasen, särskilt arsenik. Därför används vanligtvis V205. Det är mindre aktivt, men mycket billigare och förgiftas av arsenföreningar flera tusen gånger mindre än platina. Vanadinkontaktmassa innehåller 7% V205 som en aktivator - kaliumoxid, och bäraren är porös aluminiumsilikat. Katalysatorn används i form av tabletter vid t \u003d 400-600 ° C. Vid t\u003e 600 ° C inträffar en irreversibel minskning av katalysatorns aktivitet på grund av sintring av aktiva komponenter med bildning av inaktiva föreningar. Vid t< 400 0 С активность катализатора тоже падает.
Katalysprocessen äger rum i flera steg:
1.Diffusion av komponenter från kärnan av gasflödet till granulerna och in i kontaktmassans porer
2.Sorption av syre genom en katalysator.
3. absorption av SO 2 -molekyler med bildandet av SO 2 * O * Kt-komplexet
4. Omorganisering av elektroner med bildandet av en komplex SO 3 * Kt
5. Desorption av SO 3
6. Diffusion av SO3 från katalysatorkorn i gasströmmen.
Vid användning av stora katalysatorgranuler bestäms den totala processhastigheten genom diffusion (1,6 steg). Därför används vanligtvis granuler med en diameter av högst 5 mm, och i detta fall den begränsande sorptionen av SO2-molekyler (steg 2). Katalysatorns livslängd är cirka 4 år.
Flödesschema för produktion av svavelsyra.
Det tekniska systemet för produktion av svavelsyra visas i figur 1. Svaveldioxid från stekugnen går till rengöring först till cyklon 1 och sedan till torr elektrostatisk utfällare 2: gastemperaturen vid utloppet från den elektrostatiska utfällaren är cirka 300 0 C. Sedan kommer gasen in i det ihåliga tvättornet 3, där kall svavelsyra sprutas med koncentration 75%. När gasen kyls kondenseras SO 3 i den och vattenånga kondenseras till små droppar, där arsenikoxid löses upp. Som ett resultat bildas arseniksyra-dimma, som fångas upp i det ihåliga tornet 3 och i tornet med munstycket 4. Samtidigt fångas resterna av damm, selen och andra föroreningar. Slutlig SO2-rening utförs i våta elektrostatiska fällare
5. Vanligtvis installeras 2-3 filter i serie. Gasreningen slutar genom att torka den från vattenångor med koncentrerad svavelsyra i ett torn med packning 6.
Gasreningsanordningar är gjorda av rostfritt stål och dessutom fodrade med syrabeständiga tegelstenar.
Torr SO 2 och SO 3 är inte aggressiva, så resten av enheterna kan monteras i vanligt stål. Dry SO 2 kommer in i kontaktenheten, som består av:
Kontaktapparat 7
Värmeväxlare 8
Start eldgasvärmare, som används för att värma upp gasen när enheten startar eller när temperaturen sjunker.
Gas levereras till kontaktenheten med en turboladdare 9. Kontaktanordningen är en cylinder med en diameter på 3-12 m, en höjd av 10-25 m. Inuti kroppen installeras 4-5 galler med ett lager granulat av kontaktmassan. Värmeväxlare installeras mellan galler.
Färsk gas värms upp av värmen från den reagerade heta gasen i externa värmeväxlare, och därefter värms den i interna värmeväxlare till t \u003d 440-450 0 С, varefter den kommer in i det första skiktet av kontaktmassan. Efter varje lager av kontaktmassa passerar gasen genom en av de interna värmeväxlarna för kylning. Efter kontaktapparaten kommer gasen in i tornen med packning 11,12 för absorption. Absorbenten i torn 11 är oleum, och i torn 12 finns 98,3% svavelsyra, som har den bästa absorptionskapaciteten.
Absorptionen utförs med koncentrerad svavelsyra, eftersom om absorptionen utförs med vatten kommer svavelhaltig anhydrid att reagera med vattenånga för att bilda en svavelsyradimma, som är mycket svår att fånga. 

Absorptionen av svaveldioxid åtföljs av frisättningen av en stor mängd värme, vilket resulterar i att syran värms upp och absorptionen saktar ner, för att förbättra absorptionen kyls gasen och syran i en värmeväxlare. Mängden återflödessyra är många gånger större än vad som behövs för att absorbera svaveldioxid, och denna mängd bestäms av värmebalansen.
Dubbelkontaktmetod
Omvandlingen av S02 till S03 i kontaktapparaten är 90%. Resthalten av SO 2 i avgaserna är upp till 1,5%, vilket är betydligt högre än MPC. Därför matas avgaserna från absorbatorn tillbaka till kontaktanordningen. Som ett resultat ökar förhållandet O2 till SO2 och omvandlingsgraden är redan 95-97%, och SO2-halten i avgaserna är cirka 0,003%.
Användning av fast avfall från svavelsyraproduktion
Fast avfall från svavelsyraproduktion är:
1. Pyritlådor;
2. Damm från cykloner och torra elektrostatiska fällare;
3. Slam från tvättorn och våta elektrostatiska avskiljare.
Bearbetning av pyritlådor
Som ett resultat av rostning av 1 ton pyrit bildas 0,55 ton pyritslinder, som innehåller 40-63% järn, 1-2% svavel, 0,33-0,47% koppar; 0,42-1,35% zink, liksom ädelmetaller i mängden 10-20 g / ton. Extraktion av icke-järnmetaller från ask
Kloreringanvänds om kopparhalten överstiger 0,5%. Med denna metod kan du extrahera 85-90% koppar, en betydande andel ädla metaller, och ger också nästan fullständig avsvavling av askan. Kostnaden för producerad koppar täcker kostnaderna för bearbetning av askan.
Innan avfyring tillsätts upp till 20% malet natriumklorid i askan. Under rostningsprocessen bildas kopparklorid. Den optimala eldningstemperaturen är 550-600 ° C. Vid en temperatur mindre än 530 ° C bildas vattenlösligt järnsulfat i laddningen, vilket stör den efterföljande läckningen av koppar. Vid temperaturer över 600 ° C sjunker utbytet av huvudprodukterna kraftigt.
Villkor för processens optimala förlopp:
Blanda satsen;
Tillräcklig svavelhalt i askan. Svavel behövs för att omvandla natriumklorid till natriumsulfat. Om det är lite svavel tillsätts pyrit.
För att processen ska kunna starta och gå autotermiskt räcker det att värma blandningen till en temperatur av 200-300 ° C.
Processkemi
Process och barn i 3 steg:
I det första steget oxideras sulfider och järn (III) klorid bildas:
2MeS + 3O 2 → 2MeO + 2 SO 2
MeO + SO2 + 0,5O2 → MeSO 4
SO 2 + 0,5 O 2 → SO 3
Fe2 (SO4) 3 + 6 NaCl → 3Na2SO4 + 2FeCl3
I det andra steget interagerar gasfasen med laddningen med bildandet av gasformiga kloreringsmedel:
2NaCl + S02 + O2 → Na2SO4 + Cl2
4NaCl + 2 SO3 + O2 → 2Na2 SO4 + 2Cl2
2NaCl + SO3 + H2O → Na2SO4 + 2HCl
4FeCl3 + 3O2 → 2Fe2O3 + 6Cl2
2FeCl3 + 3H20 → Fe203 + 6HCl
I det tredje steget interagerar kloreringsmedel med metalloxider och sulfider:
MeS + Cl2 + 1,5O2 → MeCl2 + SO3
MeS + Cl2 + O2 → MeCl2 + SO2
MeS + 2HCl + 1,5O2 → MeCl2 + SO2 + H2O
MeO + 2HCl → MeCl2 + H2O
2Me + 3Cl2 → 2MeCl3
Som ett resultat av rostning förvandlas 85-90% av koppar till kopparklorid, som är mycket lösligt i vatten. Därför läcks koppar ut från den eldade massan med varmt vatten i flera steg: först med en lösning från tidigare operationer och sedan med utspädd syra.
Det resulterande extraktet behandlas med järnskrot. Samtidigt pågår cementeringsprocessen:
CuCl2 + Fe → Cu + FeCl2
Processen utförs utan syreåtkomst, eftersom i närvaro av syre bildas olösligt järn (III) hydroxid, som förorenar koppar.
Den använda lösningen innehåller upp till 100 g / l natriumsulfat. Det indunstas eller fryses för att erhålla natriumsulfatdekahydrat. Läckt ask torkas i mekaniska ugnar till en fukthalt av 8-10% och skickas sedan till agglomerering och masugnsproduktion. 1 ton cinder ger upp till 20 kg koppar och cirka 900 kg sinter.
Kloridsublimeringsmetod... Vid användning av denna metod behandlas askan med väteklorid i en fluidiserad bäddapparat. I detta fall släpps klorider av tungmetaller i gasfasen i fritt tillstånd.
Väteklorid kan tillföras i gasform, i form av en lösning av klorvätesyra eller i form av salter, som lätt sönderdelas eller hydrolyseras för att bilda väteklorid.
Denna teknik använder upp till tre på varandra följande enheter i det kokande skiktet: i den första enheten vid en temperatur på 600-800 ° C sönderdelas alla sulfider. I den andra reaktorn interagerar askan med väteklorid. I den tredje reaktorn skapas en reducerande miljö, på grund av vilken Fe203 passerar in i Fe3O4. Med den efterföljande magnetiska anrikningen av askan når järnhalten 70%. Askan skickas till produktion av masugnar.
De gaser som lämnar den andra reaktorn innehåller klorider av icke-järnmetaller och överskott av väteklorid. De skickas till en absorberare, där en koncentrerad lösning bildas, från vilken metaller extraheras på olika sätt. Vätekloriden som används är nästan helt regenererad.
Användning av askar vid produktion av masugnar.
Om extraktionen av icke-järnmetaller inte utförs kan pyritslindret användas omedelbart vid produktion av masugnar. Detta hindras dock av den ökade svavelhalten (upp till 3,5%) och den höga malningsgraden.
Agglomerering används vanligtvis för att minska svavelhalten och förstora askpartiklarna.
Produktion av pigment från askor och askdamm.
Att få järnbly . Flera metoder används för att erhålla rött blyjärn.
När du använder den första metodenför att erhålla rött blyjärn behandlas askan med svavelsyra vid upphettning, vilket resulterar i att järnsulfat bildas, varefter den resulterande suspensionen blandas med alabaster, krita, lera och bränns i ugnar. Beroende på bränningstemperaturen och de tillsatta tillsatserna erhålls pigment i olika nyanser.
Nackdelen med denna teknik är att svavel och dess föreningar finns i rött blyjärn, vilket gör rött bly frätande. Denna röda kabel kan inte användas för att måla metallytor.
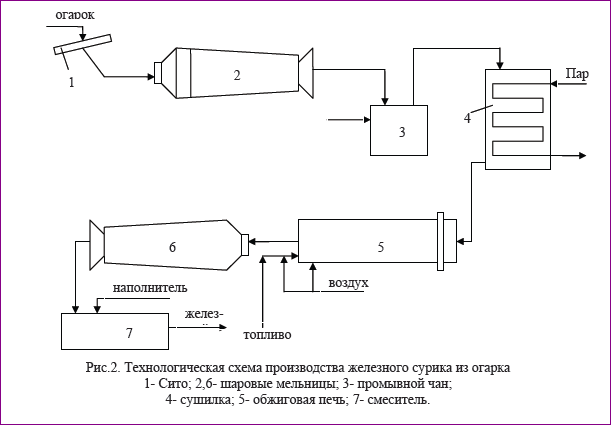
När du använder den andra metoden,vars tekniska schema visas i fig. 2; för att erhålla röd bly tas en askfraktion
0,5-2 mm, den rikaste av järnoxider. Denna fraktion matas till en kulkvarn (2). Den krossade askan tvättas med vatten i ett tvättkärl (3). Detta tar bort frätande vattenlösliga salter av järn, zink och koppar och avlägsnar delvis svavelföreningar. Tvätt utförs varmt vatten (60-80 0 ° C) under omrörning, som alternerar med smältning tills färgen orsakad av lösliga salter försvinner.
Den tvättade askan torkas med döv ånga i en torktumlare (4) och matas för bränning vid en temperatur av 850-900 ° C i en roterande ugn (5). Syftet med bränning är att ta bort fukt och svavel. Halvfärdig produkt erhållen efter bränning, som innehåller upp till 90% Fe203, males i en kulkvarn (6) och blandas med ett fyllmedel i en blandare (7). Som ett resultat erhålls rött blyjärn, som kan användas för att måla alla ytor.
Få gul ockra och mamma från askdamm. ... Askdamm avsatt i cykloner och elektrostatiska fällare innehåller mer vattenlösliga salter. Det används för att erhålla pigment som gul ockra och mamma.
Det tekniska systemet visas i figur 3. För att erhålla pigment matas askdamm in i en lösningsmedelsreaktor (1), där den blandas med vatten i 20-25 minuter. Tryckluft används för blandning. Därefter försvaras lösningen i 8 timmar. Den färgade vätskefasen pumpas ut i en mixer (2), där krita och lera tillsätts. Det är en reaktion
Fe 2 (SO4) 3 + 3CaCO3 → Fe2O3 + 3CaSO 4 + 3CO2
Resultatet är ett slam som är mättat med fukt. Den torkas i en torktumlare (5) vid 80 ° C och matas till en kulkvarn (4), från vilken den färdiga produkten kommer ut - ett torrt mineralpigment av gul ockertyp.

Vått sediment från reaktor-lösningsmedlet (1) innehållande 91% Fe203; 3,7% FeS; 5,3% föroreningar torkas vid en temperatur av 100 ° C i en torktumlare (3) och överförs sedan till en ugn (6), där svavel utbränns vid en temperatur av 800-900 ° C. En halvprodukt innehållande upp till 95% Fe203 skickas för malning i en kulkvarn (7). Lera serveras där samtidigt. Den färdiga produkten lossas från kvarnen - ett mineralpigment av mammatyp.
De resulterande mineralpigmenten är färgstabila och oförändrade över tiden. Oljefärg baserad på dem rullar inte upp och kalkfärg fäster bra.
Produktion av selen från tvättornsslam och vått
elektrostatiska utfällare.
Pyrit innehåller 0,002-0,02% Se, vilket är en kemisk analog av svavel. Därför, när pyrit avfyras, bildas förutom SO2 SeO2. Eftersom selen finns i naturen i mycket små mängder och koncentrationer är slam av svavelsyraproduktion det viktigaste råmaterialet för dess produktion. Huvuddelen av selen släpps ut med slam i tvättorn och våta elektrostatiska fällare i reningssystemet för eldgas.
Mekanismen för att separera selen från rostgaser är ganska komplicerad: vid rengöring av rostgasen absorberas SeO 2 av dimma och droppar av bevattnande svavelsyra. Lösligheten av Se02 i svavelsyra är hög.
SO2 upplöst i svavelsyra reducerar SeO2:
SeO2 + 2SO2 + 2H20 → Se + 2H2SO4
Samtidigt pågår processerna för bildning av polythioselenic syror och selenous syra:
SeO 2 + 3SO 2 + 2 H 2 O → H2 SeS 2 O 6 + H2 SO 4
SeO2 + H2O → H2 SeO3
Polythioselenic syror och selenous syra är stabila vid temperaturer som inte överstiger 70 ° C. hög temperatur de sönderfaller:
H2SO3 + 2SO2 + H2O → Se + 2H2SO4
H2SeS206 → Se + H2SO4 + SO2
Det resulterande metalliska selen fälls ut tillsammans med dammpartiklar från tvättornens syra i form av slam. Detta slam innehåller upp till 5% selen och kallas dåligt. Selen fälls också ut i våta elektrostatiska fällare. På grund av den låga dammhalten når selenhalten här 50%. Detta slam kallas rik.
Det dåliga slammet späds ut med vatten och värms upp med levande ånga för mer fullständig frisättning av selen. Den resulterande massan filtreras och den erhållna fällningen tvättas med vatten och 0,5% sodalösning. Därefter torkas slammet vid en temperatur av 90-100 ° C. Rikt slam bearbetas också. Sedan blandas båda slemmen (selenhalten är 10-12%) och matas till rostningen för att extrahera selen. Från 1 ton pyrit erhålls 10-50 g selen.
Rening av avgaser från svavelsyraproduktion
Produktionen av svavelsyra åtföljs av bildandet av aerosoler och dimma. De fastnar i dimdämpare i två steg:
I det första steget används absorberare med grova fibrer, vilket ger en rengöringseffektivitet på 90-92%
I det andra steget används absorbenter med fina fibrer, vilket ger en rengöringseffektivitet på 99,8%
SO 2 -gasutsläpp i produktionen är upp till 50 tusen ton / år.
Avgaser rengörs genom absorption med alkaliska lösningar. Lösningar av ammoniak, läsk, kalkmjölk används som absorbenter.
Ammoniaksyntes
Kväve deltar i grundläggande biokemiska processer, det är en del av proteiner. Kväveföreningar används vid produktion av mineralgödselmedel, färgämnen, plast, kemiska fibrer, läkemedel och sprängämnen. Och överallt används inte gratis kväve utan kväveföreningar. Det finns väldigt få källor av bundet kväve i naturen som är av industriell betydelse. Den största salpeterfyndigheten finns i Chile. Det finns inga sådana avlagringar i vårt land, vilket beror på den mycket höga lösligheten av kväveföreningar och det fuktiga klimatet i vårt land.
Samtidigt finns en enorm mängd kväve i den atmosfäriska luften. Därför började de leta efter sätt att omvandla atmosfäriskt kväve till dess föreningar.
Syntesen av kväveföreningar från molekylärt atmosfäriskt kväve utfördes i början av 1900-talet. tre metoder:
Arc-metod ligger i det faktum att vid ljusbågens temperatur
(2000 0 С) kväve samverkar med syre:
N2 + O2 ↔ 2NO - 179,2 kJ.
Denna metod har inte funnits bred tillämpning på grund av den låga NO-effekten och den enorma elförbrukningen för bildandet av en ljusbåge.
Cyanamidmetod ligger i det faktum att finmalt kalciumkarbid vid en temperatur av cirka 1000 ° C samverkar med kväve enligt ekvationen:
CaC2 + N2 ^ СaCN2 + C + 301kJ
Denna metod används inte heller allmänt.
Ammoniakmetod är att kväve samverkar med väte för att bilda ammoniak enligt ekvationen
N2 + 3H2 ~ 2NH3 + Q
Med denna metod är energiförbrukningen mycket mindre än de två första. Därför började denna metod användas i industriell skala. Den första ammoniakanläggningen byggdes 1913 i Tyskland.
Produktion av ammoniak med ammoniakmetoden
Metoder för att erhålla kväve
Fysisk luftseparation
Luft innehåller 78,03% -N2; 21% —02; 0,94% -Ar; och en liten mängd CO2, H2, Ne, He, Kr, Xe. Luftseparation utförs med metoden för flytande luftjustering. Metoden baseras på skillnaden i kokpunkterna för de gaser som utgör luften.
Det svåraste steget är omvandlingen av luft till flytande tillstånd. Det utförs genom att kombinera djupkylning med en ökning av trycket.
Väteproduktionsmetoder
Omvandling av metan eller naturgas händer enligt följande:
CH 4 + H2O ångor ↔ CO + 3H 2 - 206 kJ
2СH 4 + O2 ~ 2CO + 4H2 + 70kJ
CO + H2O ångor ↔ CO 2 + H2 + 41kJ
Totalt fortsätter processen med omvandling av metan med vattenånga med energiabsorption:
CH4 + 2H20-ånga ↔ CO2 + 4H 2 - 165 kJ
Metanomvandling utförs vid förhöjt tryck, vanligtvis med användning av katalysatorer. Metanhalten efter omvandling bör inte överstiga 0,5%. Den återstående metanhalten beror på temperatur, H2O: CH4-förhållande och tryck. Vid en temperatur av 800-1000 ° C uppnås den erforderliga metanhalten, men hastigheten för processen utan en katalysator är mycket låg. Därför utförs metanomvandling vanligtvis med hjälp av katalysatorer (nickelburen på aluminiumoxid). Även om metanhalten ökar med ökande tryck utförs processen ofta med ökat tryck för att öka reaktionshastigheten. I detta fall används trycket med vilket metan tränger in i anläggningen. Detta minskar energiförbrukningen för efterföljande gaskomprimering vid ammoniakproduktion.
Vid omvandlingen av kolmonoxid förblir gasvolymen konstant. Därför förändrar tryckförändringen inte jämvikten utan ökar reaktionshastigheten. En temperaturökning ökar jämvikten åt vänster, men vid låga temperaturer är reaktionshastigheten låg även i närvaro av en katalysator.
Vanligtvis utförs processen vid t \u003d 200-300 ° C i närvaro av Zn-Cr-Cu-katalysator. Den återstående CO-halten är 0,2-0,4%. Denna katalysator är mycket känslig för svavelföreningar - deras koncentration bör inte överstiga 2 mg / m 3.
Erhålla en kväve-väteblandning från koksugnsgas.
Koksugnsgas har följande sammansättning:
H2- 53%; CH4 23-28%; andra kolväten - 2-3%; CO-5-7%; C02 -1,5-2,5%;
02-0,3-0,8%; N2 \u003d 5%.
Kväveens kokpunkt är -195,7 0 C, väteens kokpunkt är -200 0 C. Alla andra komponenter har en kokpunkt över -195 0 C. Därför kyls gasen djupt till en temperatur av -195 0 C. I detta fall är alla komponenter utom kväve och väte passerar i flytande tillstånd. En del kolmonoxid finns dock kvar i den producerade gasen, vilket är ett starkt gift för katalysatorn. För att avlägsna kolmonoxid spolas gasen med flytande kväve, i vilken kolmonoxid löser sig väl. I detta fall avdunstar en del av kvävet och ett förhållande kväve till väte uppnås nära 1: 3. Sedan tillsätts kväve blandningen exakt till förhållandet 1: 3.
Rengöring av gas
En ammoniak-syntes-katalysator reduceras kraftigt i aktivitet i närvaro av svavel- och syreföreningar. Samtidigt innehåller naturgas svavelföreningar och som ett resultat av omvandlingen bildas CO 2 och CO. Innehållet av CO 2 kan nå 30% och CO - 4%. En av de svåraste uppgifterna är att rengöra gasen för dessa föroreningar till lägsta kostnad.
Gasrening från svavelhaltiga föreningar.
Naturgas innehåller följande svavelföreningar: vätesulfid, koldisulfid CS2, kolsulfid COS, merkaptaner (huvudsakligen etylmer-kaptan C2H5 -SH), den totala halten av svavelföreningar är 5-30 mg / m 3. Före rening hydreras alla svavelföreningar till vätesulfid på en kobolt-molybdenkatalysator vid t \u003d 400-450 0 С
CS2 + 4H2 → CH4 +2 H2S
COS + 4H2 → CH4 + H2S + H2O
R - SH + H2 → RH + H2S
Den resulterande vätesulfiden absorberas eller adsorberas. Som adsorbenter används: aktivt kol, järnhydroxid, zinkoxid, som absorbenter - ammoniaklösning, arsenik-sodalösningar, lösningar av natrium- och kaliumkarbonater. Den vanligaste zinkoxiden:
H2S + ZnO → ZnS + H2O
Efter absorption överskrider svavelhalten inte normen.
Gasrening från CO 2
Det finns flera sätt att rengöra gas från CO 2
Vattentvätt. När man använder denna metod spolas gasen med vatten i ett torn med en packning vid ett tryck på 20-30 atm. Vattnet som rinner ut ur tornet roterar en turbin monterad på samma axel med en pump som levererar vatten till tornet. Således återvinns cirka 60% av energin. Efter turbinen sjunker trycket till atmosfär, gasernas löslighet minskar och de släpps ut i atmosfären. Samtidigt släpps en gas som innehåller 80% CO2, 11% H2 och föroreningar - vätesulfid och kväve. Den resulterande gasen används som "torris". Efter gasutvecklingen återförs vatten till tornet.
Nackdelar med denna metod: hög energiförbrukning, höga väteförluster.
Etanolamin rening utförs med lösningar av en blandning av mono- och dietanolaminer: (CH2 - CH2 - OH) NH2 - monoetanolamin, (CH2 - CH2 - OH) 2 NH - di-etanolamin
CO 2 -borttagningsprocessen baseras på följande reaktioner:
CO2 + 2RNH 2 + H2O ↔ (RNH3) 2 CO3
CO2 + (RNH3) 2 CO3 + H2O ↔ 2RNH 3 НCO3
Absorptionsförfarandet utförs vid en temperatur av 40-45 ° C. De bildade karbonaterna och bikarbonaterna sönderdelas i stripparen med bildningen av CO2 vid en temperatur av 120 ° C.
Rengöring med varm potatislösning utförs vid ett tryck av 10-20 atm, vid en temperatur av 110-120 ° C. Vanligtvis används en 25% lösning av kaliumklorid, aktiverad med arsenik. När CO 2 absorberas omvandlas karbonat till bikarbonat
K2CO3 + CO2 + H2O ↔ 2KHCO3
Regenerering utförs med en minskning av trycket till atmosfären.
Gasrening från CO
Absorption med koppar-ammoniaklösning. Metoden baseras på det faktum att CO absorberas av en koppar-ammoniaklösning med bildandet av en komplex förening. Absorptionsförmågan hos koppar-ammoniaklösningar vid normala förhållanden små. Därför utförs rengöring vid ett tryck på 100-300 atm. och temperatur
0-15 0 C. Regenerering utförs vid en temperatur av 77-79 0 C och atmosfärstryck. Regenereringen är ännu effektivare under vakuum. Under regenerering förlorar sväljlösningen en del av ammoniak som fylls på. Efter regenerering och kylning matas absorptionslösningen åter till absorption. Efter rengöring återstår högst 0,003% CO.
Spola med flytande kväve.Vid spolning med flytande kväve löses CO i kväve. Denna metod används vanligtvis för att erhålla en kväve-väteblandning från koksugnsgas.
Teoretiska grunder för ammoniaksyntes
Syntesen av ammoniak baseras på reaktionen:
N2 + 3H2 ~ 2NH3 + Q
Reaktionen är exoterm. Reaktionsvärmen beror på temperatur och tryck. Vid en temperatur på 500 ° C beror reaktionens termiska effekt på temperaturen och trycket:
p \u003d 1 atm., Q \u003d 50 kJ / mol
P \u003d 100 atm., Q \u003d 52 kJ / mol
P \u003d 1000 atm. Q \u003d 69 kJ / mol
För att flytta jämvikten åt höger är det nödvändigt att öka trycket och sänka temperaturen. Emellertid, vid låga temperaturer, är hastigheten för processen mycket låg. Under produktionsbetingelser, för att erhålla den erforderliga hastigheten, utförs ammoniaksyntes vid en temperatur av 400-500 ° C med användning av en fast katalysator. En järnkatalysator som innehåller oxider av aluminium, kalcium och magnesium, som förstärker dess verkan, har nu blivit utbredd inom industrin. Denna katalysator uppvisade hög aktivitet och motståndskraft mot överhettning och skadliga föroreningar. Emellertid förgiftar svavelhaltiga föreningar katalysatorn irreversibelt. Med ett innehåll av 0,1% svavel i katalysatorn minskar dess aktivitet med 50%, och med ett innehåll av 1% svavel är katalysatorn helt förgiftad. Syresyrade föreningar förgiftar katalysatorn starkt, men reversibelt.
Ammoniaksyntes är en typisk heterogen katalytisk process.
De viktigaste stegen i processen:
1. Diffusion av kväve och väte från flödeskärnan till katalysatorkornet och inuti kornporerna
2.Aktiverad absorption av kväve och väte i katalysatorn.
3. Interaktion av kväve och väte på katalysatorytan, medan kväve accepterar en elektron från katalysatorn, och väte ger en elektron till katalysatorn, vilket resulterar i att följande ytkemiska föreningar bildas i följd: imid-NH, amid-NH2, ammoniak.
4. Desorption av ammoniak och dess diffusion i gasfasvolymen.
Steg 2 är den begränsande.
Faktorer som påverkar utbytet av ammoniak
Ammoniakutbytet påverkas av: tryck, temperatur, katalysatoraktivitet, rymdhastighet. Det visade sig att avlägsnandet av ammoniak från en kubikmeter katalysator ökar med sin ökning. Detta ökar emellertid volymen av den oreagerade kväve-väteblandningen. Detta ökar energiförbrukningen för gastransporter - därför väljs den optimala hastigheten utifrån ekonomiska överväganden. Vanligtvis är det 15000 h -1.
Industriella metoder för syntes av ammoniak.
Vid produktion av ammoniak används ett tryck på 100-1000 atm. och beroende på trycket, lågtryckssystem (100-150 atm.), medium
(200-600 atm.) Och hög (600-1000 atm.). I grund och botten används medeltryckssystem, eftersom problemen vid ammoniakfrigöring löses framgångsrikt med tillräcklig processhastighet. En egenskap hos ammoniaksyntes är dess låga utbyte - 14-20%
Kväve-väteblandningen som lämnar kontaktapparaten kyls medan ammoniak kondenseras och frigörs och kväve-väteblandningen återförs till apparaten. Färsk kväve-väteblandning tillsättes i erforderlig mängd.
Under återcirkulationen sker en gradvis ansamling av föroreningar, vilket leder till en minskning av katalysatorns aktivitet och som ett resultat till en minskning av produktiviteten. Föroreningarna löses delvis i ammoniak och avlägsnas från cykeln. Avlägsnande av föroreningar med ammoniak kompenserar emellertid inte för tillströmningen av föroreningar med en ny kväve-väteblandning. Därför måste en del av kväve-väteblandningen regelbundet släppas ut i atmosfären.
Syntespelarenhet
Kolonnkonstruktionen måste vara tillförlitlig och ge säker och långvarig drift.
Vid förhöjda temperaturer minskar kväve och väte stålets hållfasthet; avkolning av stål under vätepåverkan är särskilt farligt. För att sänka väggtemperaturen kommer en kall kväve-väteblandning in i kolonnen längs innerväggarna. Kroppen är gjord av krom vanadinstål, väggtjockleken är 175-200mm. Innerdiameter 1-2.8m, höjd 12-20m. Ovan och under pelaren är stängd med stålöverdrag, förstärkt med flänsar. Kolonnens utsida är värmeisolerad.
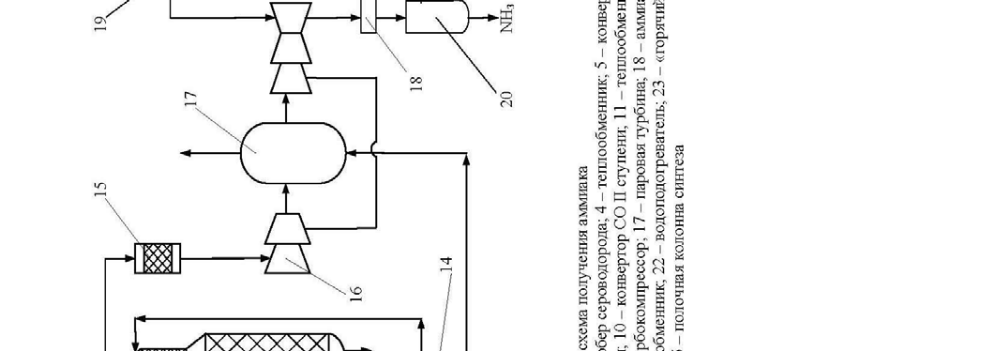
Tekniskt system för att erhålla ammoniak
Det tekniska schemat för att erhålla ammoniak visas i figur 4. Naturgas värms upp i förvärmaren 1 av avgaser och kommer in i reaktorn för hydrering av svavelinnehållande föreningar, väte matas också där. Efter hydrering kommer gasen in i adsorberaren 3 fylld med zinkoxid. Vid adsorberarens utlopp blandas gasen med ånga i förhållandet 3,7: 1, värms upp i värmeväxlaren 4 med avgaser och kommer in i rörugnen 5 med en eldstuga 6. Naturgas förbränns i eldstaden 6. Omvandlingsprocessen äger rum på en nickelkatalysator vid en temperatur av 800-850 ° C. Metanhalten efter det första omvandlingssteget är 9-10%. Vidare blandas gasen med luft och kommer in i gruvanomvandlaren 7, där restmetan omvandlas av atmosfäriskt syre vid en temperatur av 900-1000 ° C. Från gruvan omvandlas gasen till spillvärmepannan 8, där ånga med hög parameter erhålls (temperatur 480 0 C tryck - 100 atm.), riktad mot gasturbinerna i centrifugalkompressorer 17. Och gasen från spillvärmepannan går till tvåstegs CO-omvandling:
Steg 1 går i omvandlare 9 på en medeltemperatur järn-kromkatalysator vid en temperatur av 430-470 0 ° C.
Steg 2 äger rum i en omvandlare 10 på en zink-krom-kopparkatalysator vid låg temperatur vid en temperatur av 200-250 ° C. Mellan stegen passerar gasen spillvärmepannan 8.
Därefter kommer gasen in genom värmeväxlaren 11 för rengöring från syreinnehållande föreningar i skrubberen 13, bevattnad med en kall lösning av monoetanolamin, där gasen vid en temperatur på 30-40 ° C renas från CO, CO 2 och O 2. Vid absorbatorns utlopp innehåller gasen CO upp till 0,3%, CO 2 ≤ 0,003%. Gasen kommer in i metanatorn 15 för hydreringen av syreinnehållande föroreningar. Vidare kommer gasen in i ce16 driven av ångturbinen 17, där den komprimeras till ett tryck av 300 atm.
Den färska kväve-väteblandningen blandas sedan med den cirkulerande blandningen före det sekundära kondensationssystemet, som består av en ammoniakkylare 18, en separator 20, sedan passerar all denna blandning genom värmeväxlarna 21 och 23 och skickas till synteskolonnen 25.
Den reagerade gasen passerar sekventiellt genom vattenvärmaren 22, värmeväxlaren 23, luftkylaren 24, värmeväxlaren 21, kommer in i den flytande ammoniakavskiljaren 19 och kommer sedan in i kompressorn 16, där den blandas med en ny kväve-väteblandning.
Den kondenserade ammoniak avlägsnas från separatorerna 19 och 20.
Salpetersyraproduktion
Salpetersyra är en av de viktigaste mineralsyrorna, den är en tung färglös vätska. Den blandas med vatten i alla förhållanden med frisättningen av värme. Det är ett starkt oxidationsmedel. Det interagerar med alla metaller utom platinagruppmetaller. Vid interaktion med salpetersyra förstörs organiska vävnader. Utspädd HNO 3 produceras och används - 50-60% och koncentrerad - 96-98%.
Teoretiska grunder för salpetersyraproduktion
Processen att erhålla salpetersyra från ammoniak består av följande steg:
1. Kontaktoxidation av ammoniak till NO
P. Oxidation av NO till NO 2
S. Absorption av NO 2 med vatten



Bland de mineralsyror som produceras av den kemiska industrin rankas svavelsyra först när det gäller produktion och konsumtion. Detta förklaras av två skäl: dess billighet jämfört med alla andra syror och dess egenskaper. Svavelsyra röker inte, i koncentrerad form förstör inte järnmetaller, samtidigt är det en av de starka syrorna i ett brett temperaturområde
(- 40 ... - 20 260 - 336,5С) är i flytande tillstånd.
Vattenfri svavelsyra (monohydrat) är en tung oljig vätska som blandas med vatten för att producera mycket värme. Densiteten av H2SO4 vid 0 ° C är 1,85 g / cm3 och kristallisationstemperaturen är 10,7 ° C.
De största konsumenterna av svavelsyra är produktionen av mineralgödselmedel: superfosfat, ammoniumsulfat.
Många syror (fosforsyra, ättiksyra, saltsyra, koncentrerad salpetersyra etc.) och salter produceras till stor del med hjälp av svavelsyra.
Svavelsyra används i stor utsträckning vid produktion av icke-järnhaltiga och sällsynta metaller, liksom inom metallbearbetningsindustrin. Produktionen av ett antal färgämnen (för tyger), lacker och färger (för byggnader och maskiner) av medicinska ämnen och en del plast är också förknippad med användningen av svavelsyra. Med hjälp av svavelsyra, etyl och andra alkoholer produceras vissa estrar, ytaktiva ämnen och ett antal bekämpningsmedel för att bekämpa skadedjur och ogräs inom jordbruket.
Utspädda lösningar av svavelsyra och dess salter används i textilindustrin liksom i andra lätta industrier. I livsmedelsindustrin används svavelsyra för att erhålla stärkelse, melass och ett antal andra produkter. Inom elektroteknik används den som elektrolyt i batterier. Svavelsyra används för torkning av gaser och för syrakoncentration. Slutligen används svavelsyra som en komponent i reaktionsmediet i nitreringsprocesser, i synnerhet vid framställning av sprängämnen.
Under nitreringen, vid framställning av etylalkohol från eten, i koncentrationen av salpetersyra och i andra processer, används svavelsyra med en koncentration av 92 till 98% och utspädd 50 - 80% syra avlägsnas från processen. För att återföra henne till en ny mottagen cykel vattenlösningar indunstades.
Råmaterialbasen för produktion av svavelsyra är svavelhaltiga föreningar, från vilka svaveldioxid kan erhållas. Inom industrin erhålls cirka 80% svavelsyra från naturligt svavel och järn (svavelsyra) pyrit. En viktig plats i råvarubalansen upptar avgaser från icke-järnmetallurgi. Vissa industrier använder vätesulfid som råmaterial som bildas vid rening av svavel i oljeraffinering. Den första rostningen av svavelhaltiga råvaror för att erhålla svaveldioxid.
Svavelsyraproduktion innefattar följande steg av steg:
Bränning av pyrit eller svavel.
Oxidation av svaveldioxid.
Svaveltrioxidabsorption.
De ursprungliga ämnena - mineralråvaror - innehåller föroreningar, därför renas gaserna som lämnar eldningsfasen. Det första steget - rostning, är specifikt för varje typ av råvara, och vidare kommer det att betraktas för pyrit och svavel som de vanligaste utgångsmaterialen. Stegen för oxidation och absorption är i grunden desamma i olika processer för framställning av svavelsyra. Därför kommer dessa steg att betraktas som typiska processer.
Rostning av svavelhaltiga råvaror.
Rostningen av pyrit (pyrit) är en komplex fysisk-kemisk process och inkluderar ett antal sekventiella eller parallella reaktioner:
Termisk dissociation
Gasfasförbränning av svavel
Förbränning av pyrrhotit
Eller i sammandrag:
Med ett litet överskott eller brist på syre bildas blandad järnoxid
Temperatur. Termisk nedbrytning av pyrit börjar redan vid temperaturer på cirka 200 ° C och svavel antänds samtidigt. Vid temperaturer över 680 ° C fortsätter alla tre reaktionerna intensivt.
I industrin utförs rostning vid 850 - 900 ° C, när processens totala hastighet begränsas av massöverföringen av oxidationsmedlet (syre) till ytan av pyrit och nedbrytningsprodukter till gasfasen. Generellt sett kan drivkraften för denna process uttryckas av ekvationen
(1)
Det framgår av denna ekvation att faktorerna för att öka produktiviteten i processen är intensifieringen av massaöverföring (), en ökning av fasytans (F) kontaktyta och koncentrationen av reagens. Massöverföringskoefficienten kan ökas genom att öka temperaturen, fasernas kontaktyta ökar avsevärt med en ökning av graden av dispersion av det fasta materialet, och höga koncentrationer av reagens tillhandahålls genom användning av anrikad pyrit och en ökning av syrehalten i oxidationsmedlet. Man bör dock komma ihåg att en alltför hög temperaturökning främjar mjukning och vidhäftning av partiklar av fasta råvaror, och användningen av koncentrerade reagens ökar deras kostnad och leder till en alltför hög temperaturökning under förhållanden med ett autotermiskt system. Detta bestämmer valet av optimal temperatur, kombinerar tillräcklig processprestanda och användning av råvaror med lämpligt innehåll av aktiva komponenter med ett minimum av agglomereringsprocesser av fast material. I praktiken utförs processen vid en temperatur av 850 - 900С.
Tryck. I enlighet med ekv. (1) är tryck en faktor i processens hastighet, men dess tillväxt kan leda till, under autotermiska förhållanden, till en alltför hög temperaturökning och vidhäftning av partiklar av ett fast material. Dessutom leder en ökning av trycket till en ökning av kostnaden för komprimering. Eftersom avfyringsreaktionen under förhållandena med de angivna temperaturerna fortgår ganska smidigt är det att föredra att arbeta vid atmosfärstryck.
Luft-pyritförhållandet bibehålls på en nivå som ger ett överskott av syre jämfört med dess stökiometriska mängd för att uppnå höga kalcineringshastigheter, men detta överskott bör inte vara för stort, eftersom med betydande överskott överlappas ökningen av svavelåtervinningen från pyrit av en betydande utspädning av rostgaser och en minskning av koncentrationen av SO2 i dem, vilket negativt påverkar den efterföljande oxidationen av SO2 till SO3.
Tidigare var den dominerande typen av reaktor en reaktor med flera hyllor utrustad med skrapor för att jämna ut skiktet på varje hyllplan och organisera transporten av den fasta fasen från de övre hyllorna till de nedre (se typer av reaktorer för heterogena reaktioner som involverar den fasta fasen).
I en sådan reaktor är dispersionsgraden av pyrit inte hög, vilket signifikant begränsar reaktorns produktivitet. I en sådan reaktor komplicerar dessutom rörliga skrapor i högtemperaturzonen dess design, ett inhomogent temperaturregime skapas längs hyllorna och det är svårt att organisera avlägsnande av värme från reaktionszonen i den. Svårigheter vid värmeavlägsnande tillåter inte att få eldgas med en SO2-koncentration på mer än 8-9%. Huvudbegränsningen är omöjligheten att använda små partiklar, medan för en heterogen process är det huvudsakliga sättet att påskynda reaktionen partikelkrossning. Av denna anledning är anordningar för "fluidiserad bädd" av fasta partiklar mer lovande. Deras spridningsgrad gör det möjligt att påskynda processen med en storleksordning.
Pulverformig pyrit matas genom en matare till reaktorn. Oxidant (luft) matas nedifrån genom distributionsnätet med en hastighet som är tillräcklig för att väga fasta partiklar. Deras svävande i skiktet förhindrar fastnat och främjar god kontakt med gasen, utjämnar temperaturregimen genom hela skiktet, säkerställer rörligheten för det fasta materialet och dess överflöd i utloppsröret för att avlägsna cinder från reaktorn. Värmeutbyteselement kan ordnas i skiktet av rörliga partiklar. På grund av ökningen av skjutdjupet ökar SO2-innehållet i skjutgasen till 13 - 15%. Den största nackdelen med fluidiserade bäddugnar är den ökade dammigheten hos eldgasen på grund av mekanisk erosion av mobila fasta partiklar. Detta kräver en mer grundlig rengöring av gasen från damm i en cyklon och en elektrostatisk avskiljare.
Svavelförbränning.
Svavel är ett lågsmältande ämne: smältpunkten är 113С. Före förbränningen smälts den med ånga som erhålls genom att använda värmen från förbränningen. Det smälta svavlet sedimenteras och filtreras för att avlägsna föroreningarna i det naturliga svavlet och pumpas in i förbränningsugnen. Svavel brinner huvudsakligen i ångfas. För att säkerställa dess snabba avdunstning är det nödvändigt att sprida det i luftströmmen. För detta används munstycks- och cyklonugnar. De förstnämnda är utrustade med horisontella munstycken för finförstöring av vätska. I en cyklonugn matas flytande svavel och luft tangentiellt och på grund av virvelrörelsen dispergeras vätskan och de två strömmarna blandas. Små droppar avdunstar snabbt och det ångformiga svavlet brinner ut. Förbränningen fortsätter adiabatiskt och temperaturen beror på koncentrationen av SO2 som bildas.
På grund av den höga förbränningsvärmen av svavel är temperaturen i ugnen över 1000С. Dessa förhållanden är tillräckliga för avdunstning av flytande svavel. Förbränningsanläggningen arbetar tillsammans med hjälputrustning för att smälta och filtrera svavel och en spillpanna för att använda reaktionsvärmen.
Pyritristningsgaser innehåller i form av föroreningar föreningar av fosfor, selen, tellur, arsenik och några andra, bildade av orenheter av råvaror. Råvarans naturliga fuktighet förvandlas också till gas. Förbränning producerar en del SO3 och eventuellt kväveoxider. Dessa föroreningar leder antingen till korrosion av apparaten eller till katalysatorförgiftning och försämrar också svavelsyrans kvalitet. De tas bort i tvättutrymmet. Enligt schemat passerar gasen sekventiellt genom två tvättorn, bevattnade med svavelsyralösningar (60 och 20%). I det första tornet kyls eldgasen från 300 - 500 ° C till 60 - 70 ° C och frigörs från dammrester och en del av föroreningar. Detta torn är ihåligt. Dammfri gas tvättas med 15 - 20% svavelsyra från As, Fe, Se-föreningar i det andra tornet med packning. Slutlig uttorkning från fukt utförs i 3-9 torn (torkning), bevattnas med koncentrerad svavelsyra.
Oxidation av svaveldioxid.
Reaktion
Det är reversibelt och exotermt och tappar ut i volym. Det utförs på katalysatorer baserade på V2O5 med tillsats av alkalimetalloxider avsatta på kiseloxid.
Motivering av parametrarnas roll och deras val.
Temperaturen passerar den maximala prestandakaraktäristiken för reversibla exoterma reaktioner. Man bör komma ihåg att en överdriven temperaturökning kan leda till diffusionshämning av processen och detta kan påverka positionen för extremitetens produktivitet och dess värde.
Valet av temperatur bestäms till stor del av den övre och nedre gränsen för denna parameter. Vid T<400 0C активность катализаторов весьма мала, а выше 600 0С происходит их термическая дезактивация. Оптимальными являются температуры, ле-жащие внутри этих пределов.
Tryck är en faktor i processens hastighet och en faktor i förskjutning av jämvikten, men i praktiken, av energibesparingsskäl, liksom förmågan att uppnå högt utbyte och omvandlingshastigheter genom användning av andra faktorer, föredrar de att arbeta vid tryck nära atmosfären. Vissa övertryck är nödvändiga för att övervinna installationens hydrauliska motstånd när du organiserar transportflöden av reagens.
O2: SO2-förhållande. är en faktor för förskjutning av jämvikten, liksom en faktor för processens hastighet i enlighet med Boreskov-ekvationen
(2)
Uppifrån är emellertid detta förhållande begränsat av en retardation av tillväxthastigheten vid höga hastigheter och en signifikant minskning av SO2-innehållet i de kontaktgaser som tillförs till absorption, vilket minskar effektiviteten hos de senare. I praktiken används mer än ett och ett halvt överskott av O2 i förhållande till det stökiometriska.
Kontakttiden väljs utifrån den maximalt möjliga omvandlingen. Gränsen för en sådan konvertering är den maximala konverteringsgraden vid vilken hastigheten för processen är nära noll. Därför väljs den lägsta tiden under reaktionstiden vid vilken omvandlingsgraden är praktiskt taget nära jämvikten. Vanligtvis är detta värde lika med 90-95% och motsvarande tid är några sekunder.
SO2-kontaktoxidationsteknik.
Oftast i branschen används hyllenheter för att avlägsna reaktionsvärmen mellan hyllorna. Värmeväxlarplanen förutsätter maximal användning av reaktionsvärmen för uppvärmning av matargasen. I detta fall utförs avlägsnandet av värme mellan hyllorna i den utsträckning som gör att arbetstemperaturen kan bringas närmare det optimala värdet av denna parameter.
En av de viktigaste uppgifterna i produktionen av svavelsyra är att öka omvandlingen av svaveldioxid och minska dess utsläpp till atmosfären. Denna uppgift kan lösas med flera metoder.
En av de mest rationella metoderna för att lösa detta problem är dubbelkontakt- och dubbelabsorptionsmetoden (DKDA). Dess väsen ligger i det faktum att reaktionsblandningen, i vilken graden av omvandling av SO2 är 90-95%, kyls och skickas till en mellanliggande absorberare för att utvinna SO3; i den återstående reaktionsgasen ökar O2: SO2-förhållandet markant, vilket leder till en förskjutning av reaktionsjämvikten åt höger. Den nyligen upphettade reaktionsgasen matas åter till kontaktapparaten, där 95% omvandling av återstående SO2 uppnås. Den totala omvandlingsgraden av SO2 i denna process når 99,5 - 99,8%.
Svaveltrioxidabsorption.
Absorptionen av svaveltrioxid är det sista steget i processen där svavelsyra bildas. Interaktion mellan SO3 och vatten
Det flyter ganska intensivt både i vätskan och i gasfasen. Dessutom kan H2SO4 lösa SO3 i sig och bilda oleum. Denna produkt är bekväm för transport eftersom den inte korroderar ens vanliga stål. Samtidigt är svavelsyralösningar extremt aggressiva.
Jämvikts "gasvätska" för "H2O-H2SO4-SO3" visas i figur 1. Det speciella med detta system är att det i ett brett spektrum av koncentrationer av svavelsyralösning i ångfasen finns ren vattenånga och ovanför oljan - i gasfasen domineras av SO3. Samma sammansättning av vätske- och ångfaserna (azeotropisk punkt) kommer att ha en svavelsyrakoncentration på 98,3%. Om SO3 absorberas av en lösning med en lägre koncentration, fortsätter reaktion (3) också i ångfasen - en svavelsyradimma kommer att bildas, vilket lämnar absorberaren med gasfasen. Och detta är förlusten av en produkt och korrosion av utrustning och utsläpp till atmosfären. Om SO3 absorberas av oleum är absorptionen ofullständig.
Från dessa två egenskaper följer ett tvåstegsabsorptionsschema (figur 2). Gas som innehåller SO3 efter att reaktorn passerar sekventiellt oleum (1) och monohydrat (2) absorberare. Den andra komponenten i reaktionen (H2O) matas motströms genom kollektorn till monohydratabsorbatorn. På grund av den intensiva cirkulationen av vätskan (absorbera) i den är det möjligt att hålla sig nära den optimala koncentrationen av H2SO4 - 98,3% (ökningen av koncentrationen per vätskepassage är inte mer än 1 - 1,5%). Absorptionskoncentrationsförhållanden säkerställer fullständig absorption av SO3 och minimal bildning av svavelsyradimma. Syran från monohydratabsorbatorn kommer in i oleum. Det cirkulerar en 20% lösning av Н2SO4, som delvis tas som slutprodukt - oleum. Ki-slots från en tidigare absorberare - monohydrat - kan också vara en produkt. Kylskåp finns i cirkulationssystemet för att avlägsna reaktionsvärmen och ge effektivare absorption. Vid temperaturer under 100C absorberas SO3 nästan helt, svaveldioxid absorberas praktiskt taget inte.
Utsikter för utveckling av svavelsyraproduktion.
En ökning av koncentrationen av svaveldioxid är ett kraftfullt sätt att öka produktiviteten för svavelsyraproduktion. Högkoncentrerade gaser som innehåller upp till 80% SO2 har redan börjat erhållas vid produktion av icke-järnmetaller från deras sulfidmalmer med hjälp av tekniskt syre.
Produktionen av högkoncentrerad svaveldioxid gör det möjligt att skapa energiteknisk cyklisk produktion av svavelsyra från svavel och pyrit. Svaveldioxid erhållen med användning av tekniskt syre oxideras med 90% i en kontaktapparat med en "fluidiserad bädd" -katalysator. Efter absorption av SO3 erhålls högkoncentrerat oleum och monohydrat. Efter absorption återgår gasen till kontakt. I reaktorn är den totala omvandlingen 99,995%. För att avlägsna kväve som ackumulerats som ett resultat av multipelåtervinning, passeras en del av gasen efter absorption genom en liten svavelsyraanläggning, från vilken kväve släpps ut i atmosfären. Arbetsintensiteten hos ett cykliskt system som arbetar under ett tryck av cirka 1 MPa med syre är tiotals gånger högre än intensiteten hos konventionella system. Förlust av svavel med avgaser och därmed utsläpp av SO2 och SO3 till miljön minskas också tio gånger.
Systemen tillhandahåller alstring av vattenånga (4 MPa) på grund av eldgasernas värme, som kan användas både i själva installationen för att kompensera för energikostnader för drift av kompressorer och pumpar och i andra verkstäder på anläggningen. Värmen från svavelgaser efter att ha passerat genom nästa katalytiska skikt kan användas för förvärmning av reagensen vid inloppet till kontaktanordningen. Sorptionsvärmen används för hushållsbehov.
De viktigaste riktningarna för utvecklingen av svavelsyraproduktionen är:
1. Öka kraften i utrustningen med samtidig komplex automatisering av produktionen.
2. Intensifiering av processer genom användning av reaktorer med fluidiserad bädd (både vid rostningsstadiet och i kontaktoxidation av SO2), mer aktiva katalysatorer, ökat tryck och användning av tekniskt syre i oxidationsprocessen.
3. Utveckling av krafttekniska system med maximal användning av värme från exoterma reaktioner, inklusive cykliska system under tryck.
4. En ökning av omvandlingsgraden i alla produktionsstadier för att minska konsumtionsfaktorerna för råvaror och material och minska skadliga utsläpp.
5. Användning av skadliga utsläpp från avgaser samt fast avfall (cinder). Exempelvis kan oönskade föroreningar H2S och SO2 från olika strömmar kombineras och koncentreras för att omvandla dem till elementärt svavel.
Den hårda askan som innehåller järnoxid kan användas som ett absorberande medel för att fånga upp gaser och behandla avloppsvatten.
