
















 Назад вперед
Назад вперед
Увага! Попередній перегляд слайдів використовується виключно в ознайомлювальних цілях і може не давати уявлення про всі можливості презентації. Якщо вас зацікавила дана робота, будь ласка, завантажте повну версію.
Мета уроку:
Навчальні цілі: Актуалізувати знання про метали: стан в Періодичній системі, особливості будови атомів, фізичні властивості. Вивчити стан неметалів в Періодичній системі і особливості будови їх атомів. Повторити кристалічну будову неметалів, а отже, розглянути їх фізичні властивості.
Виховують мети: Створювати умови для формування в учнів здатності слухати один одного, аналізувати і доповнювати відповіді товаришів.
Розвиваючі цілі: Сприяти розвитку в учнів логічного мислення, сприяти вмінню учнів описувати властивості речовин.
устаткування: Зразки неметалів, наявні в лабораторії.
Тип уроку: Водний урок, урок вивчення нових знань.
Методи, що застосовуються на уроці:
- Евристична бесіда.
- Антитеза - протиставлення одних об'єктів природи іншим: неметалів металів.
- Спостереження (описати властивості речовин по фотографіях).
Хід уроку
I. Організаційний момент.
II. Введення в тему уроку.
Учитель починає урок з демонстрації першого слайда (Слайд 1) і питання учням:
Що зображено на фотографіях?
Розгляньте фотографії та згадайте, яку тему ви вивчали до сьогоднішнього уроку?
Відповідь учнів:
- метали.
Сьогодні почнемо вивчати речовини, які використовуються для виготовлення предметів, зображених на другому слайді (Слайд 2).
Які це речовини?
Відповідь учнів:
- Неметали.
Отже - тема уроку « Загальна характеристика неметалів » (Слайд 3).
3. Загальна характеристика неметалів
Властивості і хімія елементів-неметалів є більш складними і різноманітними в порівнянні з такими для металів.
Сьогодні ми будемо порівнювати властивості металів і неметалів, і протягом уроку записувати свої висновки в таблицю 1 (Слайд 4).
Таблиця 1. Порівняння властивостей металів і неметалів.
| характеристика | метали | Неметали | |
| 1. Хімічні елементи | |||
| Положення в Періодичній системі | |||
| Особливості будови атомів | 1. Кількість електронів на зовнішньому електронному шарі | ||
| 2. Радіус атома | |||
| 3. Окисно-відновні властивості | |||
| 2. Прості речовини | |||
| Тип хімічного зв'язку | |||
| Кристалічна решітка | |||
| Загальні фізичні властивості | 1. Стан при звичайних умовах | ||
| 2. Колір | |||
| 3. Блиск | |||
| 4. Пластичність або крихкість | |||
| 5. Тепло- та електропровідність | |||
Таблиця представлена \u200b\u200bна слайдах, і ми зможемо перевіряти правильність протягом уроку.
а. Положення неметалів в ПС.
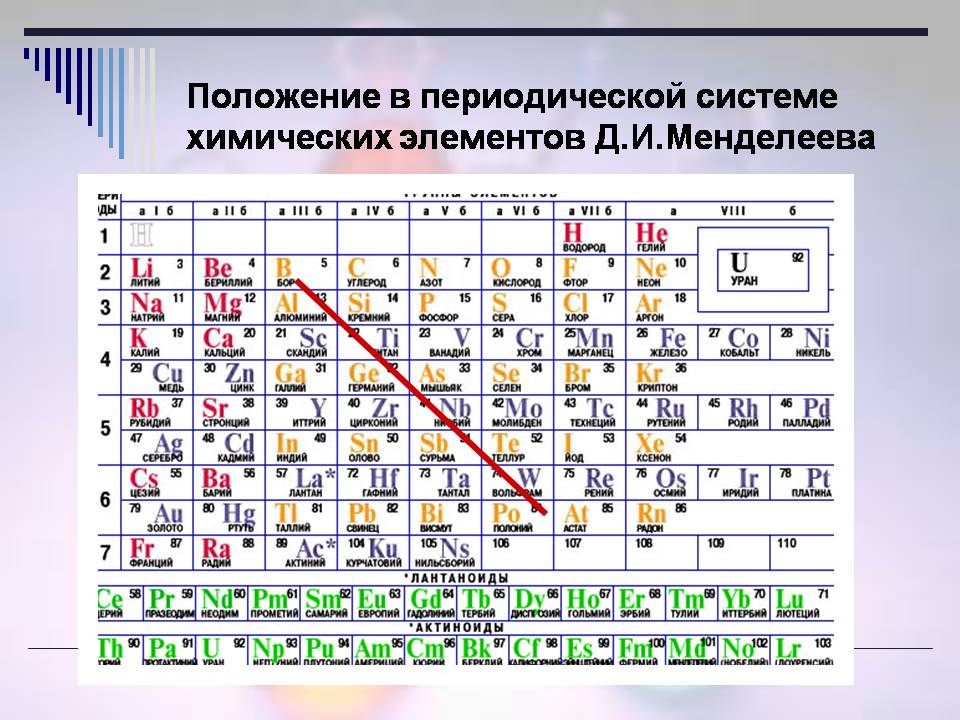
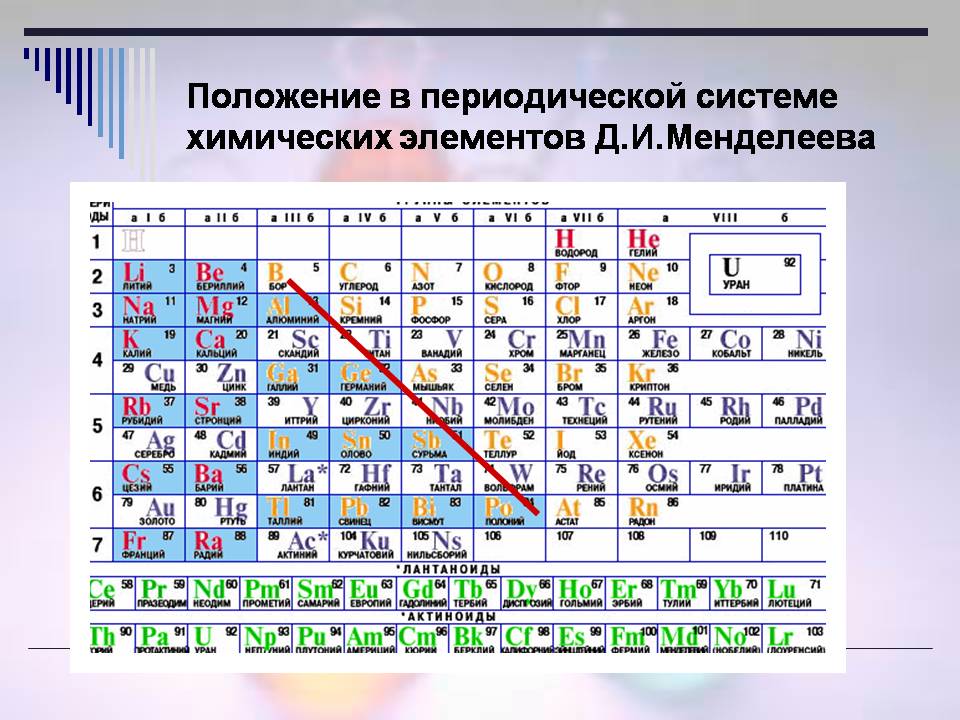
Розглянувши ПС, згадайте, де знаходяться метали (Слайди 5, 6 і 7)?
Відповідь учнів:
- У головних підгрупах нижче діагоналі В - At
- У побічних підгрупах
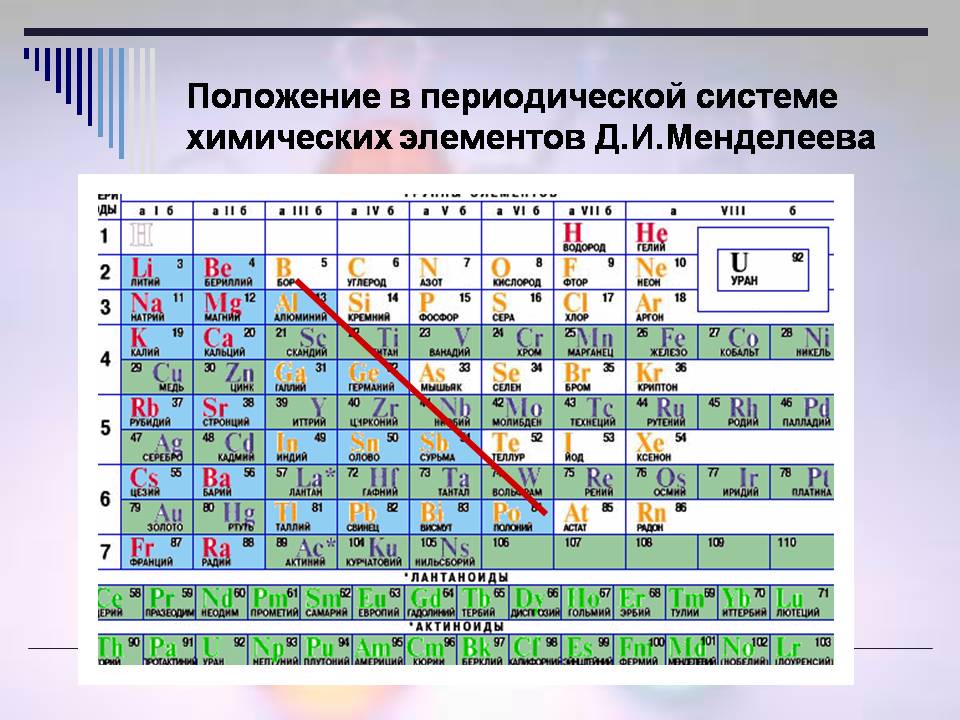
Тоді, де ж знаходяться неметали (Слайд 8)?
Відповідь учнів:
- Неметали розташовані в правому верхньому куті ПСХЗ (уздовж і над діагоналлю В - At).
Всього 22 елемента є неметалами в періодичній системі.
Запишемо в таблицю.
б. Особливості атомної будови елементів-неметалів.
Тепер розглянемо особливості будови атомів.
Питання: запишемо схеми будови атомів, елементів, записаних на дошці (Слайд 9).
У правій колонці - метали, в лівій - неметали.
Розглянемо зовнішній шар:
Відповідь учнів:
- У металів ....
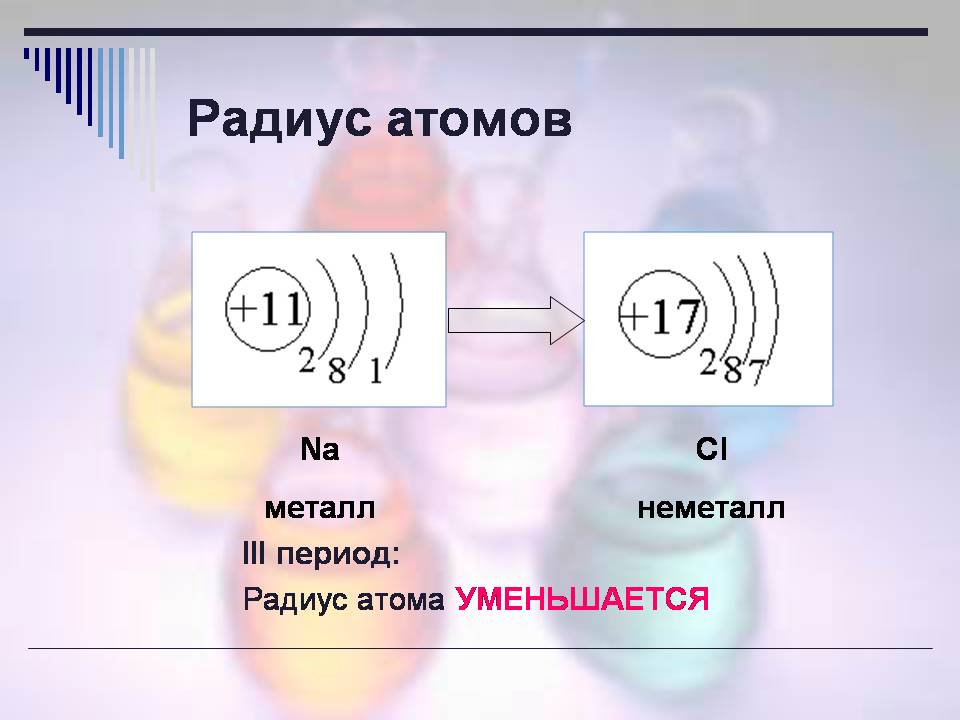
Наступна характеристика: радіус атома.
Розгляньте картинки (Слайд 10) і дайте відповідь на питання: які це елементи, що спільного в їх розташуванні в ПС?
Відповідь учнів:
- Це елементи натрій і хлор, розташовані в 3 періоді.
Як змінюється радіус атомів в періоді?
Відповідь учнів:
- Зменшується.
Т. е. У неметалів радіус менше.
Запишемо в таблицю.
Переходимо до окисно-відновних властивостях.
Згадаймо - метали проявляють ... .. відновлювальні .... властивості.
А неметали?
Відповідь учнів:
- Окисні.
Розберемося?
Розглянемо реакції горіння деяких неметалів в кисні.
Детальніше розберемо горіння сірки. Запишемо рівняння, баланс (Слайд 11).
Тобто неметали і окислювачі і відновники.
Ми роздивились хімічні елементи, Перевіримо таблицю (Слайд 12).
в. характеристика простих речовин неметалів.
Тепер переходимо до простих речовин.
Працюємо з другою частиною таблиці (Слайд 13).
Перше - тип зв'язку.
Який зв'язком утворені прості речовини метали?
Відповідь учнів:
- металевої
Неметали?
Відповідь учнів:
- Ковалентного неполярной.
Записали.
Який тип кристалічної решітки у речовин з металевим зв'язком (Слайд 14)?
Відповідь учнів:
- металева
Ковалентного неполярной? Перш, ніж відповісти, зверніть увагу на малюнки. Див. Слайд.
Відповідь учнів:
- Атомна або молекулярна.
Записали.
Кристалічна решітка визначає фізичні властивості речовин.
Згадаймо фізичні властивості речовин з металевою решіткою.
По таблиці.
А які у неметалів. Розглянемо (Слайди 15-17).
Тепер перевіримо наші записи (Слайд 18).
III. Повторення.
на зворотному боці листа поставте в стовпчик п'ять цифр, і дайте відповідь «Так» або «Ні» на запитання представлені на слайді (Слайд 20).
перевіримо (Слайд 21).
У кого все правильно - підніміть руку.
В кінці уроку вчитель може виставити оцінки найбільш активним учням.
висновок:
Неметали - хімічні елементи, атоми яких мають велике число електронів на зовнішньому електронному шарі, малий радіус і мають переважно окислювальні властивості.
Неметали - прості речовини не володіють фізичними властивостями металів, проявляють велику різноманітність у властивостях, що пояснюється різними типами кристалічних решіток.
слайд 5 з презентації «Метали і неметали». Розмір архіву з презентацією 137 КБ.
Хімія 8 клас
короткий зміст інших презентацій«Кислоти 8 клас» - Згадайте, що ми знаємо про кислотах на прикладі. Подумайте! www.undersky.ru. H2CO3. images.yandex.ru. www.sunhome.ru. Металу (неметалла) солеобразующіе (несолеобразующіе) Кислотний (основний). Прохорова Світлана Миколаївна. Дайте характеристику оксидів.
«Солі 8 клас» - Назвіть речовини: Складне речовина, що складається з іона металу і кислотного залишку. Дати назву: MgSO4 Al2 (SO4) 3 Fe (NO3) 3 CaCO3 NaCl. Хімія - 8 клас. Склади формулу: З переліку виписати: Оксиди; Основи; Кислоти. Оксидами Підставами Кислотами. Урок хімііі в 8 класі по темі: Caco3 - мармур, вапняк, крейда. Що називається: Сіль -. Мета уроку: CaO Ca (OH) 2 HNO3 Al2 (SO4) 3 H3PO4 CO2 H2S NaCl Mg (OH) 2 CaCO3.
«Будова речовини хімія» - Гази, рідини, тверді тіла. Як змінювалися уявлення про атомах з плином часу? Автор однієї з моделей отримав Нобелівську премію двічі. Кластер найважливішою молекули на Землі. Як вчені дізнаються про будову речовини? Атомний рівень організації речовини. Чи завжди атоми менше молекул? Речовина і тіло. Молекули. Що таке атом? МОУ Ліцей № 40 БУДОВА РЕЧОВИНИ. Назвіть імена вчених, які вивчали (вивчають) будова речовини. Браун, Лемей. Що таке молекула?
«Урок Кисень» - Купцова А.А.Методіческая розробка уроку з хімії «Кисень. Передмова. Цілі: Тому робота з учнями вимагає від вчителя постійного методичного технічного вдосконалення. Готую презентації до уроків, щоб урізноманітнити форми уроків хімії учнів. У запропонованій методичній розробці представлена \u200b\u200bрозробка уроку «Кисень. ІКТ надає велику допомогу також при підготовці і проведенні уроків. Випуск 2./Под загальною редакцією Н.В.Борісовой. - Чебоксари, 2010. - 208 с.).
«Речовина в хімії» - Кисень. Речовини. Вода Залізо Кисень Мідь Алюміній Хлорофіл Цукор. Здатність реагувати з іншими речовинами. Дерево. Водень. Хімічні. Проста речовина. Сьогодні ми починаємо вивчати одну з найдавніших з важливих наук-хімію. Метан. Учитель: Харгелюнова І.Г. МОУ Виноградненська ЗОШ. Прості. Ацетон. Тверді речовини. Метал. Вільні атоми.
«Складні і прості речовини» - Більшість металів мають сірим, сріблясто білим кольором. Прості речовини. Сірка, хлор, алмаз і багато інших є представниками неметалів. Складні речовини. Над презентацією працювала Патокин Юлія учениця 8-Б кл. Відомо понад 80 різних металів. Утворення складного речовини з простих називається синтезом. Визначення складу складного речовини шляхом розкладання називається аналізом. Метали.
