
















 العودة إلى الأمام
العودة إلى الأمام
احترام! يتم تضمين العرض الأمامي للشرائح لأغراض إعلامية فقط وقد لا ينقل جميع ميزات العرض التقديمي. إذا كان هذا الروبوت قد خدعك، من فضلك، من فضلك، إغرائي بإصدار جديد.
تعريف الدرس:
الأهداف الأولية:تحديث المعرفة حول المعادن: مراحل الجدول الدوري، خصائص الذرات الطبيعية، القوة الفيزيائية. احسب موقع العناصر غير المعدنية في الجدول الدوري وخصائص ذراتها. كرر التركيب البلوري لللافلزات، ثم انظر إلى قواها الفيزيائية.
فيخوفويوت ميتي:تكوين عقول للصياغة في المجال العلمي والاستماع لبعضهم البعض والتحليل وتوسيع أنواع الأصدقاء.
أهداف التطوير:قبول تنمية التفكير المنطقي لدى الطلاب، وقبول قدرة الطلاب على وصف قوة الخطابات.
تركيب الحمام:علامات اللافلزات الموجودة في المختبر.
نوع الدرس:درس الماء، درس تعلم المعرفة الجديدة.
الأساليب التي يجب اتباعها في الفصل:
- محادثة ارشادية.
- النقيض - معارضة بعض الأشياء في الطبيعة للآخرين: اللافلزات والمعادن.
- الحذر (وصف قوة الخطب من الصور الفوتوغرافية).
تقدم الدرس
I. اللحظة التنظيمية.
ثانيا. مقدمة لموضوع الدرس.
يبدأ المعلم الدرس بمظاهرة الشريحة الأولى (شريحة 1)والغذاء للدراسة:
ما هو مبين في الصور؟
انظر إلى الصور وخمن ما هو الموضوع الذي تعلمته قبل درس اليوم؟
تقرير الطالب :
- معدن
حان الوقت اليوم لتعلم الكلمات المستخدمة في عرض العناصر على الشريحة الأخرى. (الشريحة 2).
أي نوع من الكلام؟
تقرير الطالب :
- لم يكونوا معدنيين.
أوتجي - موضوع الدرس " خاصية الزجالنيغير المعادن » (الشريحة 3).
3. خصائص اللافلزات
تعتبر قوى وكيمياء العناصر غير المعدنية أكثر تعقيدًا وتنوعًا من تلك الخاصة بالمعادن.
اليوم سوف نقوم بموازنة قوة المعادن واللافلزات، وطوال الدرس سوف نسجل النتائج التي توصلنا إليها في الجدول 1 (الشريحة 4).
الجدول 1. معادلة قوى المعادن واللافلزات.
| صفة مميزة | معدن | غير المعادن | |
| 1. العناصر الكيميائية | |||
| المواقف في الجدول الدوري | |||
| ملامح ذرات المستقبل | 1. عدد الإلكترونات الموجودة على الكرة الإلكترونية الحالية | ||
| 2. نصف القطر الذري | |||
| 3. الطاقة القائمة على الأكسيد | |||
| 2. اغفر الكلمات | |||
| نوع الموثق الكيميائي | |||
| شبكة كريستال | |||
| السلطات المادية القبيحة | 1. معسكر مع أعظم العقول | ||
| 2. اللون | |||
| 3. بليسك | |||
| 4. اللدونة أو الصلابة | |||
| 5. الحرارة والتوصيل الكهربائي | |||
يتم عرض الجدول على الشرائح، ويمكننا التحقق من صحة الدرس.
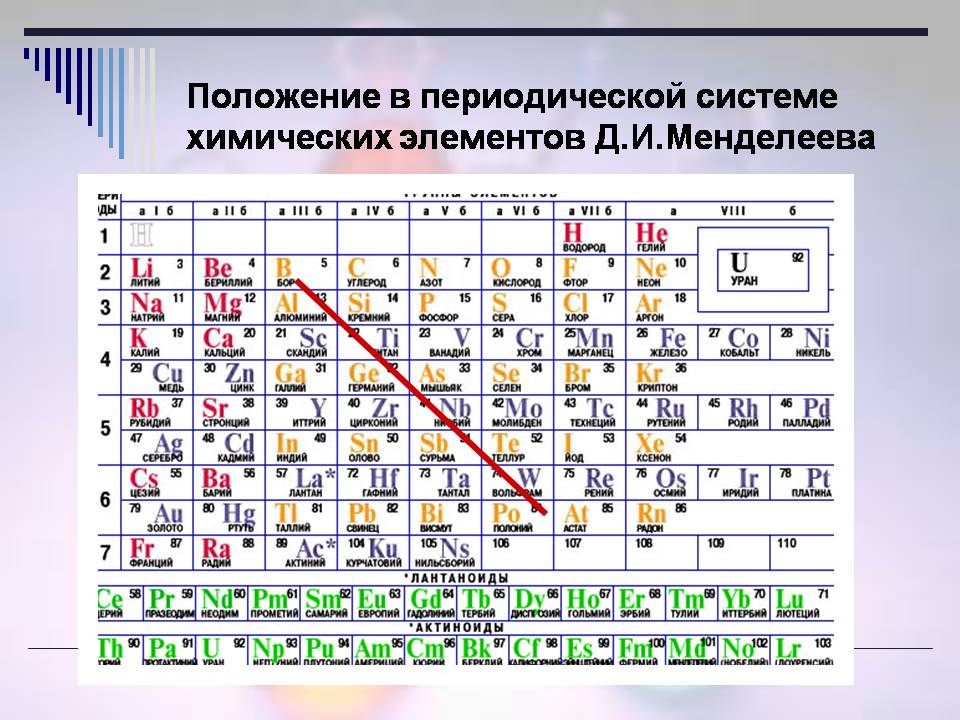
أ. موقف اللافلزات في PS.
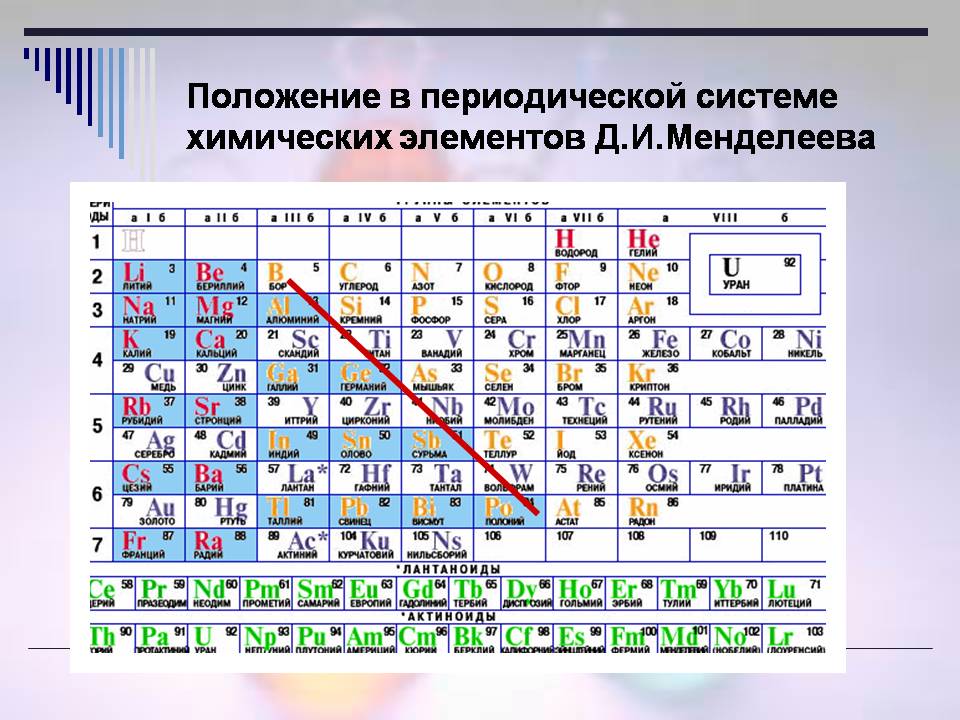
بعد أن نظرت إلى PS، خمن أين سيعرفون (الشرائح 5 و6 و7)?
تقرير الطالب :
- المجموعات الفرعية الرئيسية لها أقطار أقل B - At
- في مجموعات فرعية ثانوية
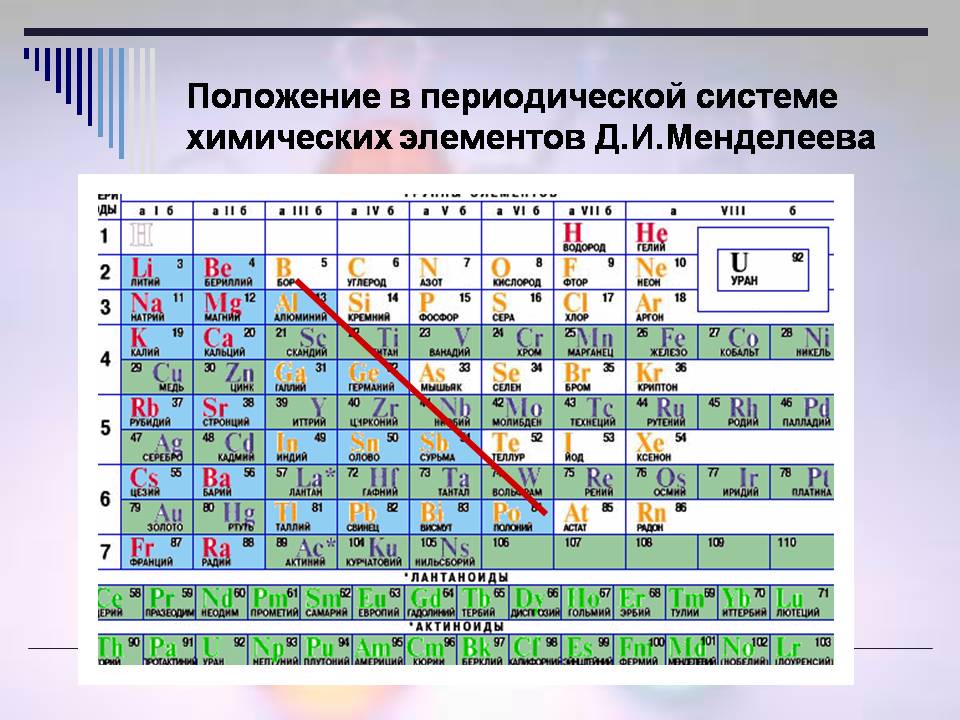
تودي، أين تعرف اللافلزات؟ (الشريحة 8)?
تقرير الطالب :
- يتم سحق المواد غير المعدنية في الزاوية اليمنى العليا من PSHZ (العقدة وفوق القطر B - At).
إجمالي 22 عنصرًا غير معدني في الجدول الدوري.
دعونا نكتبها في الجدول.
ب. مميزات العناصر المعدنية الذرية غير المعدنية.
الآن دعونا نلقي نظرة على خصوصيات الذرات اليومية.
التغذية: دعونا نكتب مخططات الذرات والعناصر المكتوبة على السبورة (الشريحة 9).
يحتوي العمود الأيمن على معادن، بينما يحتوي العمود الأيسر على مواد غير معدنية.
دعونا نلقي نظرة على الكرة الخارجية:
تقرير الطالب :
- في المعادن....
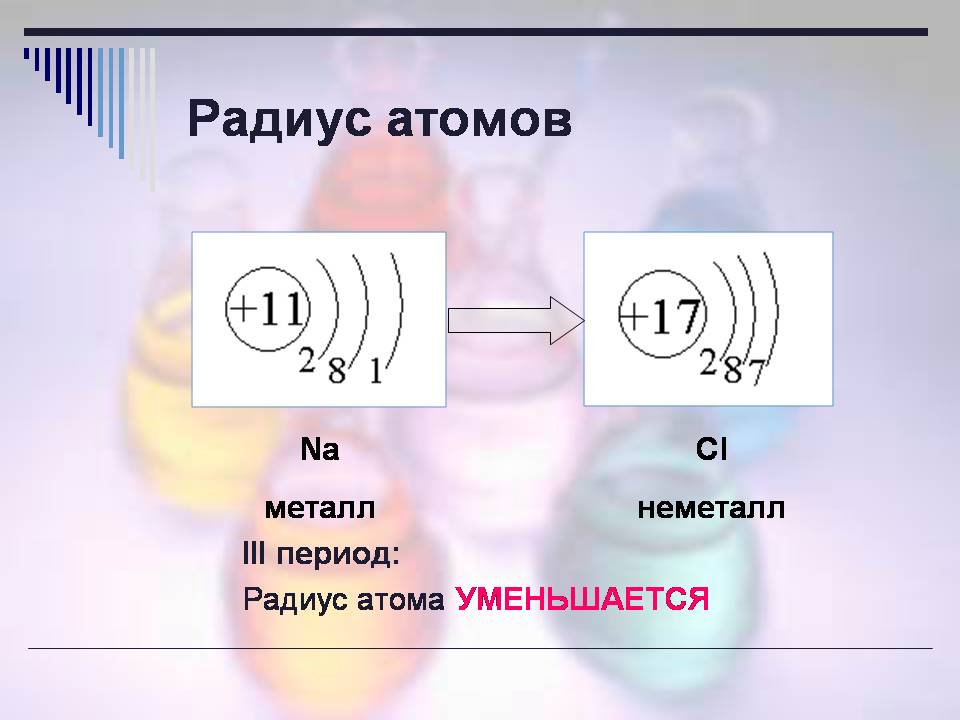
الخصائص المتاحة: نصف القطر الذري.
أنظر إلى الصور (الشريحة 10)وإعطاء إجابة على التغذية: ما هي العناصر الصحية الموجودة فيها المزروعة في PS؟
تقرير الطالب :
- عنصري الصوديوم والكلور، يذوبان على 3 مراحل.
كيف يتغير نصف قطر الذرات مع مرور الوقت؟
تقرير الطالب :
- التغييرات.
أي أن المواد غير المعدنية لها نصف قطر أصغر.
دعونا نكتبها في الجدول.
دعنا ننتقل إلى السلطات القائمة على الأكسيد.
زغاديمو - ميتال للعرض... .. حب.... قوة.
ماذا عن غير المعادن؟
تقرير الطالب :
- أكسيد.
هل سنحمل؟
دعونا نلقي نظرة على تفاعل الفرن مع مختلف المعادن غير الحمضية.
دعونا نلقي نظرة فاحصة على جبل سيركا. دعونا نكتب، التوازن (الشريحة 11).
وكانت هذه المعادن غير المعدنية، سواء المؤكسدات أو المؤكسدات.
فوجئنا العناصر الكيميائية، دعونا نتحقق من الجدول (الشريحة 12).
الخامس. صفة مميزة خطابات بسيطةغير المعادن.
الآن دعنا ننتقل إلى الخطب البسيطة.
عملت مع جزء آخر من الجدول (الشريحة 13).
بيرشي هو نوع من الارتباط.
ما نوع التماسك الذي أحدثته الخطب البسيطة؟
تقرير الطالب :
- معدن
هل لم المعادن؟
تقرير الطالب :
- تساهمية غير قطبية.
مسجل.
أي نوع شعرية الكريستالفي الأنهار مع اتصال معدني (الشريحة 14)?
تقرير الطالب :
- ميتاليفا
تساهمية غير قطبية؟ أولاً، لنفترض أن نجلب الاحترام للصغار. شعبة. الانزلاق.
تقرير الطالب :
- الذرية أو الجزيئية.
مسجل.
تشير الشبكة البلورية إلى القوة الجسدية للخطابات.
نحن نعرف القوة الجسدية للخطب بشبكة معدنية.
حسب الجدول.
ماذا عن غير المعادن؟ لنلقي نظرة (الشريحة 15-17).
الآن دعونا نتحقق من سجلاتنا (الشريحة 18).
ثالثا. يكرر.
على حارس البوابةورقة، ضع خمسة أرقام في العمود، ثم أعط الإجابة "نعم" أو "لا" للعرض التقديمي المقدم على الشريحة (الشريحة 20).
دعونا إعادة التحقق (الشريحة 21).
من لديه كل شيء على ما يرام، يرفع يده.
في نهاية الدرس، يمكن للمدرس إعطاء الدرجات للطلاب الأكثر نشاطا.
فيسنوفوك:
اللافلزات هي عناصر كيميائية تحتوي ذراتها على عدد كبير من الإلكترونات في كرة إلكترونية خارجية ونصف قطر صغير ولها قوة مؤكسدة مهمة.
غير المعادن - فقط لا تتحدث بصوت عالٍ السلطات الماديةتظهر المعادن تنوعًا كبيرًا في قوتها، وهذا ما تم توضيحه أنواع مختلفةالمشابك الكريستال.
الشريحة 5مع العرض "المعادن وغير المعادن". حجم الأرشيف مع العرض التقديمي هو 137 كيلو بايت.
الكيمياء الصف الثامن
المدى القصيرالعروض الأخرى"الأحماض الصف الثامن" - خمن ما نعرفه عن الأحماض الموجودة في المؤخرة. يفكر! www.undersky.ru. H2CO3. image.yandex.ru. www.sunhome.ru. معدن (غير معدني) مكوّن للملح (غير مكوّن للملح) حمض (أساسي). بروخوروفا سفيتلانا ميكولايفنا. إعطاء خصائص الأكاسيد.
"الأملاح الصف الثامن" - تسمية الكلام: كلام مركب يتكون من أيونات المعادن وفائض الأحماض. سمها: MgSO4 Al2 (SO4) 3 Fe (NO3) 3 CaCO3 NaCl. الكيمياء - الصف الثامن. أضف الصيغة: اكتب من الفائض: أكسيد؛ الأساسيات؛ الأحماض. الأكاسيد والمواد والأحماض. درس الكيمياء في الصف الثامن حول موضوع: Caco3 - مرمور، فابنياك، كريدا. ما يسمى : سيل - . تعريف الدرس: CaO Ca (OH) 2 HNO3 Al2 (SO4) 3 H3PO4 CO2 H2S NaCl Mg (OH) 2 CaCO3.
"كيمياء الكلام بودوفا" - الغازات والسوائل والمواد الصلبة. كيف تغيرت الظواهر المتعلقة بالذرات مع مرور الوقت؟ فاز مؤلف أحد النماذج بجائزة نوبل لشخصين. مجموعة من الجزيء الأكثر أهمية على وجه الأرض. كيف يعرف الناس دائمًا الكلام اليومي؟ الراوند الذري لتنظيم الكلام. هل الذرات أصغر من الجزيئات؟ الكلام والجسد. الجزيئات. ما هي الذرة؟ المؤسسة التعليمية البلدية صالة حفلات رقم 40 BUDOVA RECHOVYNY. اذكر أسماء التلاميذ الذين رددوا (رددوا) الخطب اليومية. براون، ليماي. ما هو الجزيء؟
"درس كيسن" - كوبتسوفا أ.أ. التطوير المنهجي لدرس الكيمياء "كيسن. بيريدموفا. الأهداف: لذلك فإن العمل مع الطلاب يتطلب دقة فنية منهجية وثابتة من المعلم. أقوم بإعداد العروض التقديمية قبل الدروس من أجل فهم أشكال دروس الكيمياء للطلاب بشكل واضح. يتم عرض التطوير المنهجي المقترح في درس "Kisen. توفر تكنولوجيا المعلومات والاتصالات أيضًا مساعدة كبيرة في إعداد الدروس وإجرائها. العدد 2./تحت التحرير الرسمي لـ N. V. بوريسوفا. - تشيبوكساري، 2010. - 208 ص).
"الكلام في الكيمياء" - كيسن. ريشوفيني. ماء زاليزو كيسن نحاس ألومنيوم كلوروفيل تسوكور. ومن المهم الرد على الخطب الأخرى. شجرة. فودين. المواد الكيميائية مجرد خطاب. اليوم نبدأ بدراسة أحد أهم العلوم وهو الكيمياء. الميثان. المعلم: كارجيليونوفا آي جي. المؤسسة التعليمية البلدية Vynogradnenska Zosh. آسف. الأسيتون. كلام حازم. معدن. ذرة فيلني.
"الخطب القابلة للطي والبسيطة" - معظم المعادن لها لون أبيض رمادي فضي. اعذروني على الكلام. الكبريت والكلور والماس وغيرها الكثير ممثلون للمواد غير المعدنية. خطب قابلة للطي. عملت يوليا باتوكين، طالبة الصف الثامن، على العرض التقديمي. نرى أكثر من 80 معدنًا مختلفًا. أوسفيتا خطاب قابل للطييسمى ببساطة التوليف. يسمى التعيين إلى مستودع الكلام القابل للطي عن طريق التفريغ بالتحليل. يرمي.
